北京基因組所揭示新靶點NOTCH4在人巨核細胞發育和再生中的重要作用
近日,中國科學院北京基因組研究所精準基因組醫學重點實驗室王前飛研究組與美國約翰霍普金斯大學醫學院程臨釗教授合作,揭示了NOTCH4作為轉錄因子RUNX1的靶基因調控體外巨核細胞發育,并篩選出可促進體外巨核細胞再生的小分子抑制劑。該研究不僅找到了體外巨核細胞再生的新靶點,并且提供了一種利用罕見病尋找再生靶點的新思路,相關成果受邀在第58屆美國血液學年會上做口頭報告,并獲得該年會的摘要成就獎,論文發表于血液領域最有影響力的Blood 雜志。新靶點NOTCH4及其抑制劑的醫藥用途已申請國內及國際專利。
巨核細胞(MK)是骨髓中高度多倍體化且高效生成血小板的重要細胞,而血小板在止血、傷口愈合以及維持機體穩態等過程中具有重要作用。轉錄因子RUNX1單等位基因胚系突變會引起MK發育障礙和血小板減少的家族性血小板疾病(FPD),但具體機制尚不清楚。程臨釗教授前期工作發現利用FPD病人來源的多能干細胞(hiPSCs)體外模型可重現病人表型,而通過基因打靶修復RUNX1 突變后可以恢復其巨核細胞的生成能力。
為了揭示FPD巨核發育障礙和血小板減少的發病機制,促進體外巨核細胞/血小板再生,王前飛研究組利用疾病干細胞體外模型結合功能基因組學,找到了一系列受RUNX1調控并對巨核細胞生成具有重要作用的靶基因和通路。其中,首次揭示NOTCH4作為轉錄因子RUNX1的直接靶基因,負向調控體外巨核細胞發育;并篩選出Notch通路的小分子抑制劑,使得從多能干細胞和臍血來源的造血干祖細胞,生成巨核細胞的產量提高近十倍。該成果有望應用于臨床輸注,治療包括血小板減少癥、腫瘤化療后、手術外傷出血等在內的多種凝血功能障礙疾病,具有較高的科學意義和臨床價值。
該研究獲得了中科院國際合作局對外合作重點項目、自然科學基金委、中科院青年創新促進會、中科院王寬誠教育基金會等的資助。
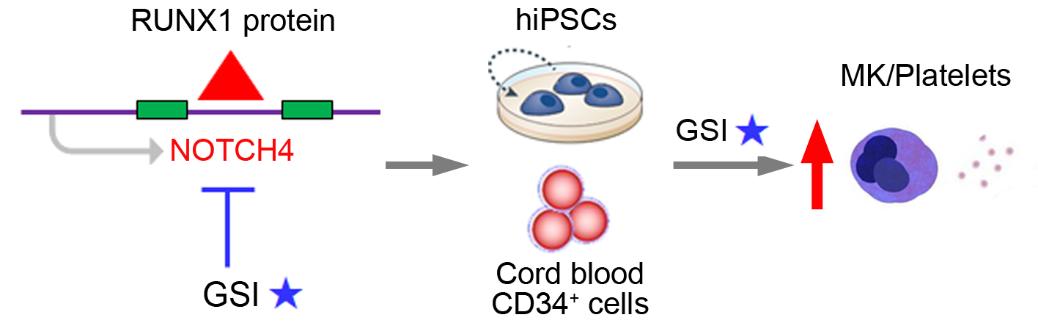
新靶點可促進體外巨核細胞再生