基因組所RNA m6A甲基化調控mRNA剪切研究獲新進展
6-甲基腺嘌呤【N6-methyl-adenosine(m6A)】是高等生物mRNA中含量最為豐富的甲基化修飾形式之一,發生于保守序列RRACH(R=G ,A; H=A,C or U)中,富集在mRNA的外顯子編碼區及3’-非編碼區。類似于DNA甲基化修飾,RNA的m6A甲基化修飾也是可逆的,由m6A甲基轉移酶復合物METTL3/METTL14/WTAP催化形成 (Ping XL. et al. Cell Res 2014),并由去甲基化酶FTO(Jia G. et al. Nat Chem Biol 2011)和ALKBH5(Zheng G. et al. Mol Cell 2013)負責去除,運輸到細胞質m6A修飾的mRNA能夠被YTHDF2識別而降解。而在細胞核內,m6A修飾如何調控mRNA加工還不清楚。
近日,中國科學院北京基因組研究所精準基因組醫學重點實驗室楊運桂研究組研究發現,m6A去甲基化酶FTO調控mRNA剪切加工和脂肪細胞分化,該研究成果在Cell Research在線發表。
科研人員利用細胞生物學、基因組學、生物信息學等多層次技術手段,發現了m6A去甲基化酶FTO缺失可阻礙脂肪前體細胞3T3-L1的分化;在3T3-L1細胞分化過程中,m6A修飾不僅在外顯子剪切位點附近高富集,還和mRNA剪接加工重要因子SR蛋白結合序列具有空間重疊性;FTO的缺失可增加外顯子剪切增強子結合蛋白SRSF2對RNA的結合能力,促進SRSF2靶基因的外顯子保留;FTO調控轉錄因子RUNX1T1第六位外顯子的可變剪切產物,調控了脂肪前體細胞3T3-L1分化。上述研究結果提示了依賴于m6A去甲基化酶FTO的mRNA m6A修飾作為一種新的順式調控元件,在細胞核內可以調控mRNA剪切加工和脂肪細胞分化。
該研究成果為后續研究m6A的生物功能和RNA表觀遺傳提供了依據,為從RNA甲基化這一新角度展開肥胖癥等人類疾病的發生發展研究提供了理論依據。
該項工作得到了中國科學院、科技部、國家自然科學基金委的資助。
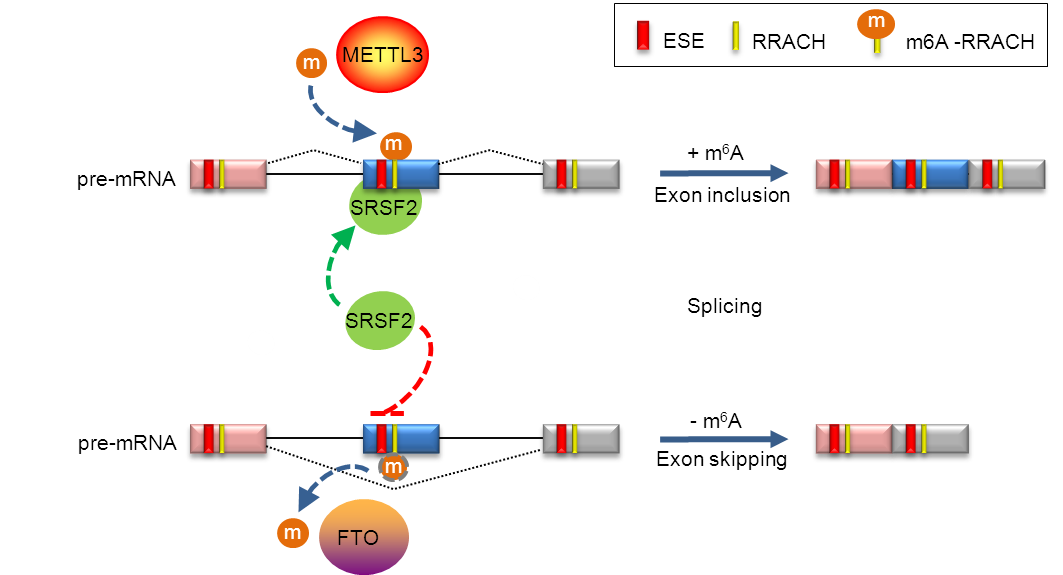
依賴于m6A去甲基化酶FTO的mRNA m6A修飾促進外顯子剪切增強子結合蛋白SRSF2對RNA的結合能力,
增加SRSF2靶基因的外顯子保留